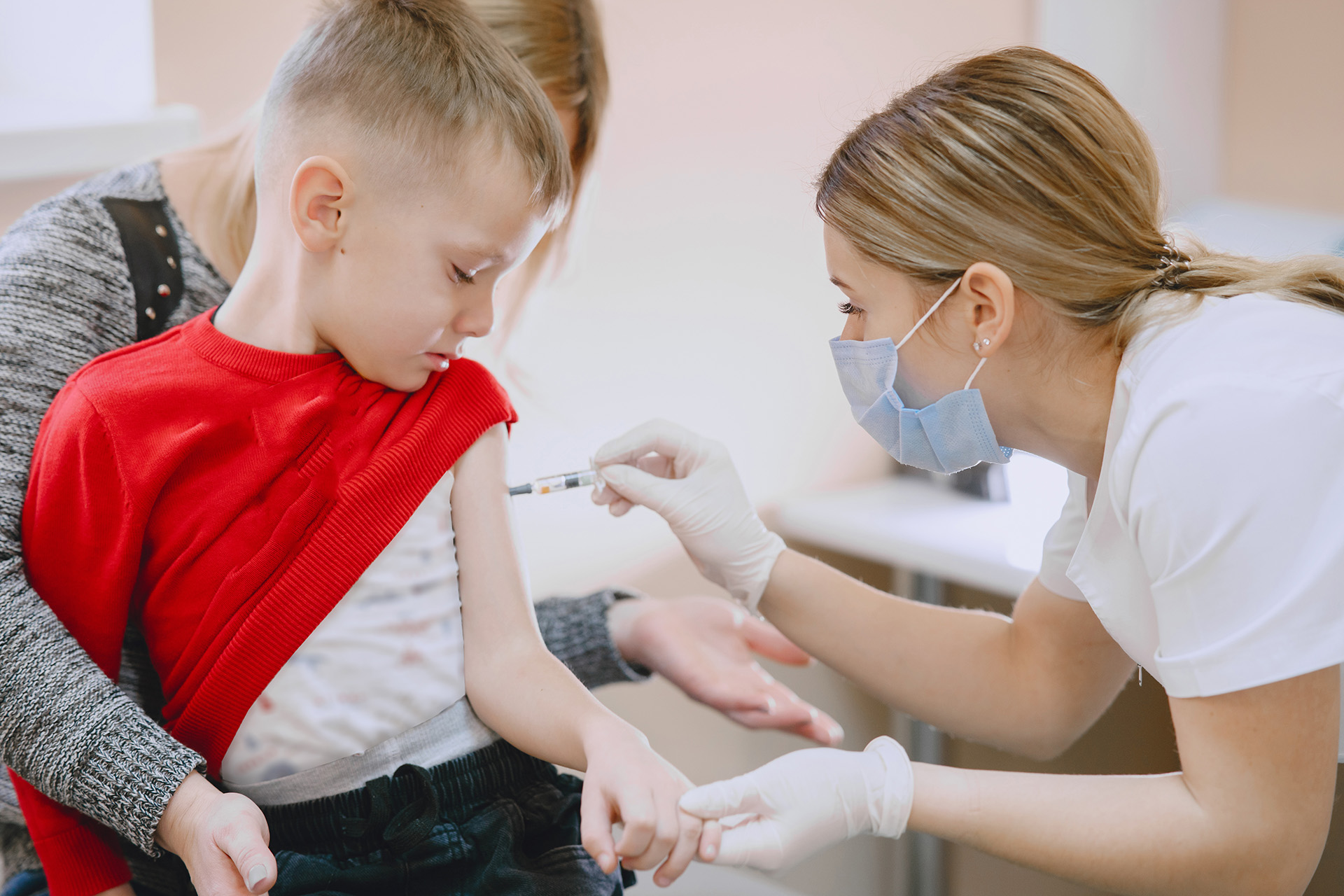
VPH: Un paso más hacia la igualdad gracias a la vacunación
El Dr. Francisco Giménez, director del Instituto Balmis de Vacunas, da su visión sobre la vacuna del VPH en La Voz de Galicia.

El Dr. Francisco Giménez, director del Instituto Balmis de Vacunas, da su visión sobre la vacuna del VPH en La Voz de Galicia.

El encuentro anual, organizado por el Instituto Balmis de Vacunas, se celebrará los días 10 y 11 de noviembre en formato presencial y online.
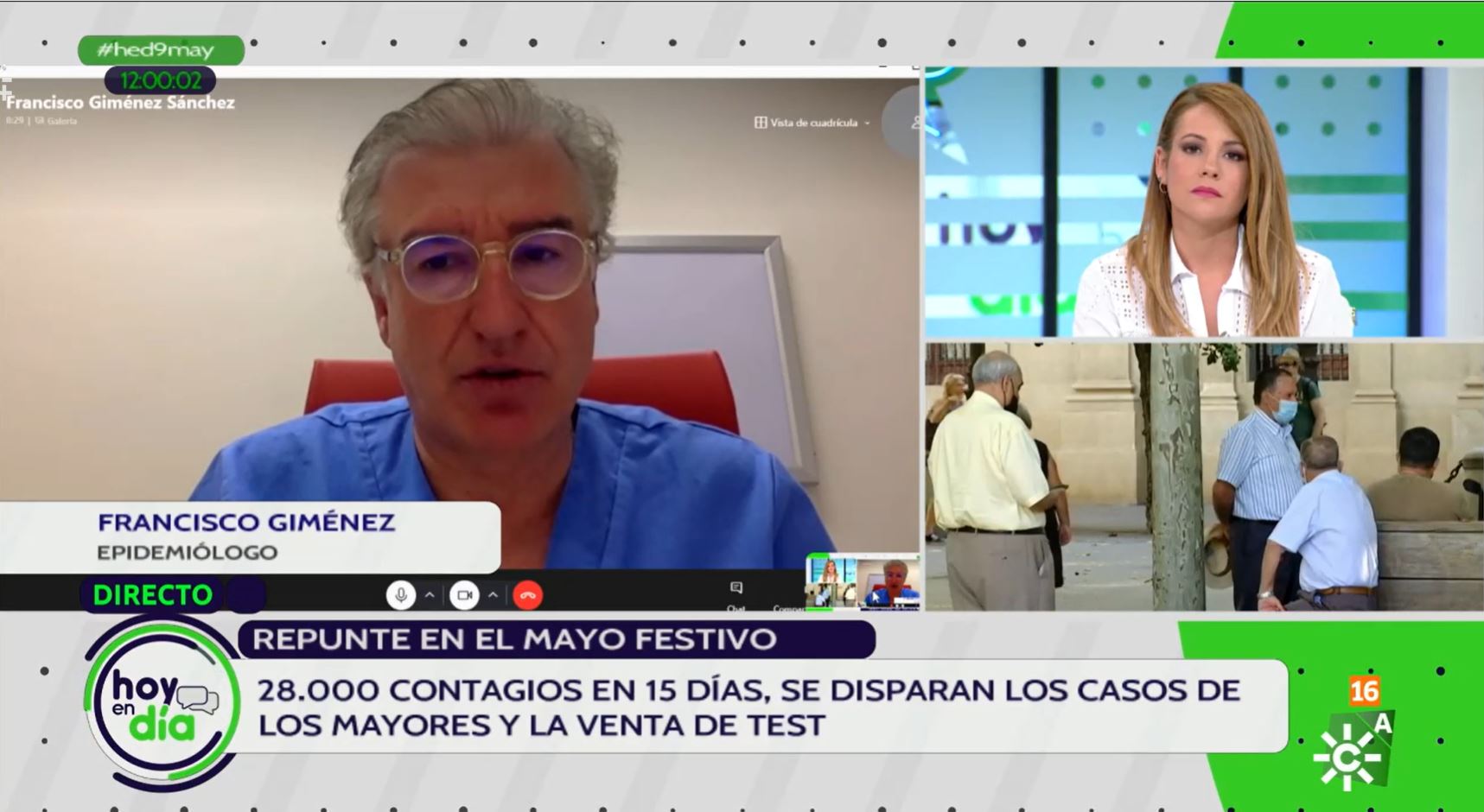
El director del Instituto Balmis de Vacunas valora la situación epidemiológica de Andalucía en una entrevista en el programa Hoy en día de Canal Sur TV.

El Instituto Balmis de Vacunas destaca que la inclusión de la vacuna contra el Virus del Papiloma Humano en niños en el calendario vacunal de Cataluña es un hito sanitario.

Si te perdiste alguna sesión puedes ver el vídeo en este artículo.

Se celebra del 24 al 30 de abril con el objetivo de concienciar sobre la importancia de las vacunas para proteger contra enfermedades prevenibles.
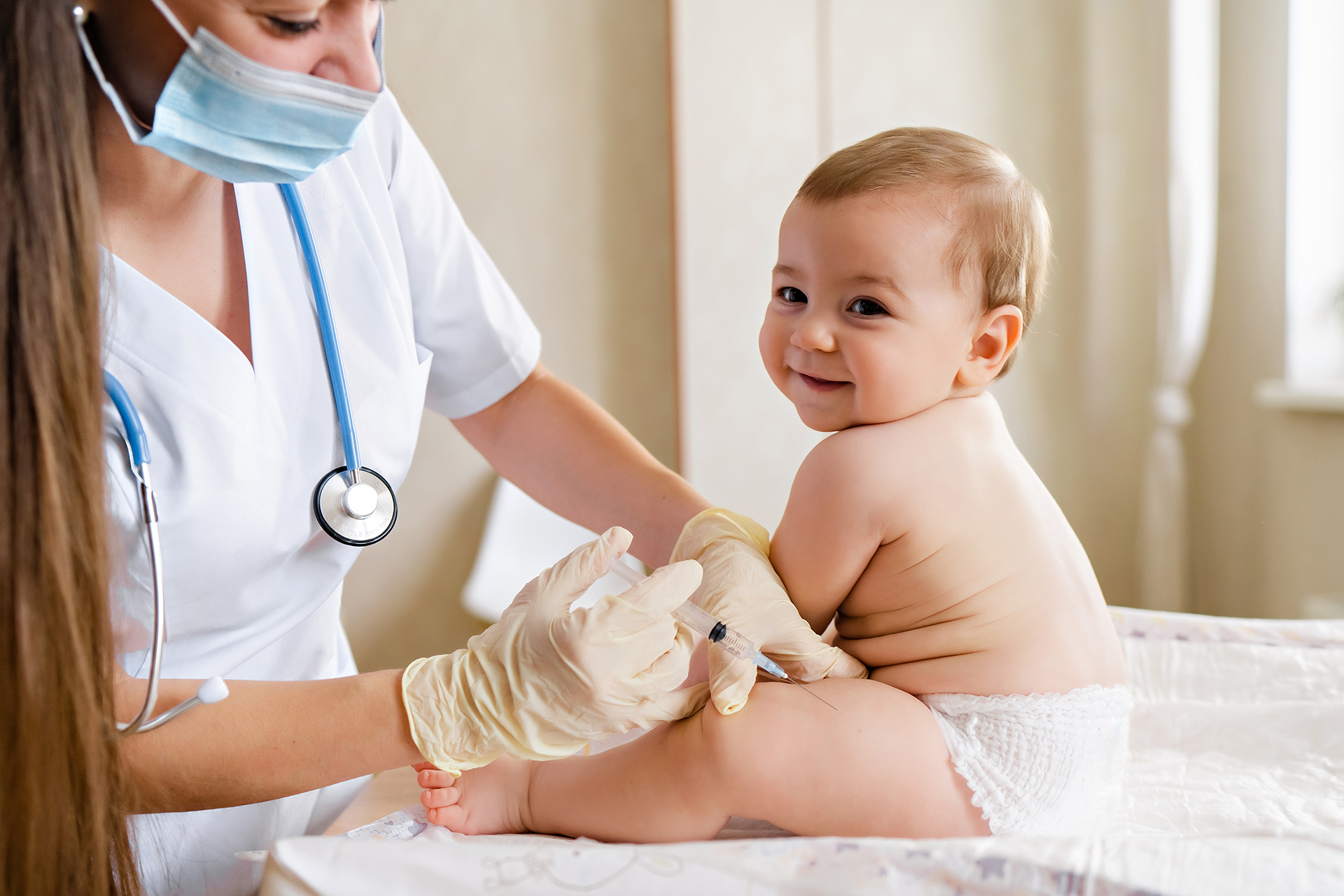
Con motivo del Día Mundial contra la Meningitis, el Dr. Francisco Giménez Sánchez insta al gobierno nacional y los autonómicos a incluir la vacuna contra el meningococo B en sus calendarios vacunales gratuitos, como ya están haciendo algunas regiones

Con la incidencia actual, el Dr. Francisco Giménez explica que “hay que ser prudentes especialmente en sitios poco ventilados y con aglomeraciones, al menos hasta que las cifras estén en niveles bajos”.
Organizado por GRINDOPE Barcelona, se celebrará de manera presencial y online los días 26, 27 y 28 de mayo.

Con el nombre ‘Vacunas y vacaciones: el papel de la inmunización en la reactivación del turismo’, el encuentro online se celebrará el próximo 10 de mayo.

Contemplan un cambio en el sistema de contabilidad de la Covid que ya no registrará todos los casos positivos, por lo que la incidencia descenderá debido a la falta de notificación de casos sin que los datos se ajusten a la realidad.
Expertos en vacunología han abordado la situación actual de la vacunación y las últimas recomendaciones sobre inmunización.

Teléfono: 670717505
Email: secretaria@ibvacunas.com
Almería (España)
Copyright 2024. Instituto Balmis de Vacunas. Política de privacidad y aviso legal.
Sitio web realizado por AOM Comunicación y Marketing Digital
Este sitio web utiliza cookies para que usted tenga la mejor experiencia de usuario. Si continúa navegando está dando su consentimiento para la aceptación de las mencionadas cookies y la aceptación de nuestra política de cookies, pinche el enlace para mayor información. ACEPTAR