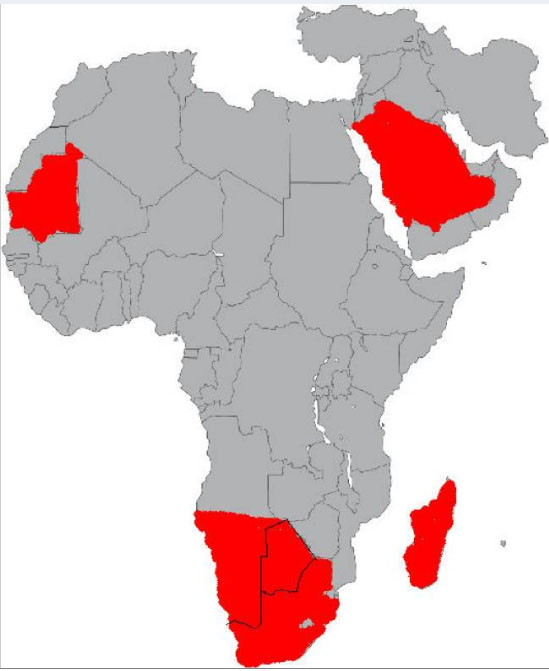
El virus de la fiebre del valle del Rift es un patógeno transmitido por artrópodos que se distribuye en diversas áreas geográficas del este de África subsahariana. Originariamente la enfermedad fue relacionada exclusivamente con el ganado, sin embargo la descripción de casos en humanos con evolución fatal, ha renovado el interés por el estudio de esta entidad (1).
El virus es transmitido por una variedad de mosquitos que incluyen las especies Aedes, Culex y Anopheles. Aunque la fiebre del valle del Rift esta en la actualidad limiatada a las regiones subsaharianas del este, los vectores capaces de transmitir la enfermedad se encuentran en en el sudeste de Europa y en Norteamérica. Además el virus puede sobrevivir en los huevos de mosquito, resistiendo periodos prolongados de aridez.
 La epidemias periódicas de fiebre del valle del Rift han motivado en el pasado pérdidas en la industria ganadera local; sin embargo no es hasta hace un par de décadas que la comunidad internacional toma conciencia de los daños potenciales que esta enfermedad puede ocasionar. Recientemente este virus se ha clasificado como potencial agente bioterrorista, lo que ha renovado e interés por su estudio y el desarrollo de medidas profilácticas que pudieran permitir el control de epidemias en el futuro. Ya se han descrito casos esporádicos en turistas alemanes y de otros países europeos, por lo que diversas organizaciones sanitarias consideran que es cuestión de tiempo que el virus de la fiebre del valle del Rift comience afectar la ganadería de países del sudeste de europa, donde la clomatologia puede similar a las delas zonas de origen. El virus de la fiebre del valle del Rift es un Flebovirus que pertenece a la familia buyanviridae. El virus tiene un genoma con una sola cadena de RNA, dividida en tres segmentos, los segmentos L y M tienen polaridad negativa, el tercer segmento, S, tiene una polaridad ambivalente. El segmento L codifica la RNA polimerasa viral, usada para la transcripción del RNAm. El segmento M codifica dos glicoproteínas Gn y Gc, así como una `proteína no estructural o de fusión (Nsm1) con Gn, dando lugar a NSm2. El segmento S codifica nucleoproteínas, complementarias a las proteínas no estructurales NSs. Cuando se ensamblan los nuevos viriones en la célula, se liberan envueltos de una bicapa lipídica. El tamaño de los viriones es de 80-100 nm, están compuestos de subunidades de heterodímeros de Gn y Gc, formando cubiertas icosaédricas de 122 capsómeros.
La epidemias periódicas de fiebre del valle del Rift han motivado en el pasado pérdidas en la industria ganadera local; sin embargo no es hasta hace un par de décadas que la comunidad internacional toma conciencia de los daños potenciales que esta enfermedad puede ocasionar. Recientemente este virus se ha clasificado como potencial agente bioterrorista, lo que ha renovado e interés por su estudio y el desarrollo de medidas profilácticas que pudieran permitir el control de epidemias en el futuro. Ya se han descrito casos esporádicos en turistas alemanes y de otros países europeos, por lo que diversas organizaciones sanitarias consideran que es cuestión de tiempo que el virus de la fiebre del valle del Rift comience afectar la ganadería de países del sudeste de europa, donde la clomatologia puede similar a las delas zonas de origen. El virus de la fiebre del valle del Rift es un Flebovirus que pertenece a la familia buyanviridae. El virus tiene un genoma con una sola cadena de RNA, dividida en tres segmentos, los segmentos L y M tienen polaridad negativa, el tercer segmento, S, tiene una polaridad ambivalente. El segmento L codifica la RNA polimerasa viral, usada para la transcripción del RNAm. El segmento M codifica dos glicoproteínas Gn y Gc, así como una `proteína no estructural o de fusión (Nsm1) con Gn, dando lugar a NSm2. El segmento S codifica nucleoproteínas, complementarias a las proteínas no estructurales NSs. Cuando se ensamblan los nuevos viriones en la célula, se liberan envueltos de una bicapa lipídica. El tamaño de los viriones es de 80-100 nm, están compuestos de subunidades de heterodímeros de Gn y Gc, formando cubiertas icosaédricas de 122 capsómeros.
En las dos décadas transcurridas desde la caracterización del virus de la fiebre del valle del Rift, se ha podido desarrollar una cepa neurotrópica (cepa de Smithburn) considerablemente atenuada que se ha utilizado como vacuna en el ganado y ha demostrado inducir una potente respuesta protectora frente al virus, por desgracia también origina abortos en el ganado con relativa frecuencia y parece especialmente patógena para los caballos europeos; por ello en la actualidad se reserva sólo para controlar los brotes epidémicos.
Los candidatos vacunales para ser utilizados frente al virus de la fiebre del valle del Rift se pueden clasificar en cuatro grupos: vacunas atenuadas, inactivadas, recombinación viral y vacunas DNA.
Vacunas atenuadas. Además de la cepa de Smithburn, dos candidatos se han desarrollado demostrando mayor protección y menos virulencia en el huésped: MP12 y Clon 13. La MP12 es una cepa atenuada desarrolada de la cepa egipcia del virus ZH548, que fue asilada de un paciente humano. Se creó tras 12 pases en presencia del mutágeno 5-fluoracilo. Esta vacuna es efectiva en corderos y caballos y parece estar especialmente indicada en zonas donde la fiebre del valle del Rift es endémica, el inconveniente es que al igual que la cepa de Smitburn, puede inducir abortos en corderos.
Vacunas inactivadas. Tienen la ventaja de inducir inmunidad protectora, sin el riesgo de las vacunas atenuadas de que la actividad mutágenica revierta la patogenicidad disminuida del virus. La inactivación se realiza con formalina y como inconveniente, requieren de multiples inoculaciones para obtener respuestas protectoras adecuadas.
Partículas virus-like. Generadas por genética reversa o expresión de vectores en células eucariotas. Ofrecen la ventaja de poder expresar elementos inmunogénicos del virus sin el riesgo de la replicación del virus, las comunicaciones existentes en la actualidad parecen coincidir en que la expresión de partículas virus-like es factible en líneas celulares de mamífero y confieren protección en el modelo murino de experimentación.
Vectores virales recombinantes. Ofrecen dos ventajas potenciales sobre las vacunas convencionales. Es posible la expresión de los genes de nuestro interés sin necesidad de la infección viral, los antígenos recombinantes de nuestro interés no se expresan en los huéspedes naturales del virus, eliminando los riesgos de la infección por virus atenuados. Se han expresado Gn y Gc del virus en una vacuna DNA que inoculada al ratón le confirió inmunidad protectora. Las glicoproteínas del virus también se han incorporado a un vector viral del tipo vaccinia de Ankara.
Dr. José Uberos Fernández
Hospital Clínico San Cecilio de Granada
REFERENCIAS
(1) Boshra H, Lorenzo G, Busquets N, Brun A. Rift valley fever: recent insights into pathogenesis and prevention. J Virol 2011 Jul;85(13):6098-105.