El citomegalovirus tiene una alta seroprevalencia en la población humana con niveles de infección que llegan al 95% en países desarrollados. Tras la infección inicial el virus permanece de forma latente en las células progenitoras CD34 de médula ósea y en monocitos, pudiendo reactivarse con posterioridad. En el huésped inmnocompetente y la reinfección es habitualmente asintomática, en el huésped inmunodeprimido la infección por citomegalovirus es una importante causa de morbilidad y mortalidad. Pudiendo ocasionar un amplio espectro de enfermedad, desde neumonitis, lesiones gastrointestinales, hepatitis, sordera, microcefalia y retinitis. Recientemente la infección por citomegalovirus se ha relacionado con algunas variedades de cánceres y enfermedades inflamatorias como la enfermedad de Crohn y la colitis ulcerosa. Durante los primeros 3 meses de vida la eliminación de citomegalovirus en orina se ha relacionado con la severidad de la enfermedad. A finales de la década de los 80 se desarrolló el primer método no basado en cultivo celular para la cuantificación de partículas virales. El método de antigenemia se basó inicialmente en el uso de anticuerpos monoclonales frente al antígeno p72 de citomegalovirus, identifica de esta forma células que contienen este antígeno en sangre. Posteriormente el método se modificó para detectar la fosfoproteina pp65 de citomegalovirus. Este método se ha utilizado para detectar leucocitos infectados en sangre periférica y se considera un marcador de infección diseminada, con un valor predictivo positivo cercano al 70%. Sin embargo, el mayor avance en el desarrollo de las técnicas de cuantificación de la infección por citomegalovirus se produce con las técnicas de reacción en cadena de la polimerasa (PCR), estas técnicas poseen una sensibilidad mucho mayor que las técnicas de cultivo celular y antigenemia anteriormente comentadas: Las primeras técnicas de PCR eran esencialmente cualitativas, posteriormente se pudo realizar la cuantificación del número de partículas introduciendo una cuantificación interna del estándar, que abrieron las puertas a las determinaciones de PCR en tiempo real.
Debe quedar claro que el establecimiento de enfermedad por citomegalovirus debe ir precedido por la replicación del virus, los pacientes que tienen una carga viral elevada tienen un riesgo elevado de desarrollar enfermedad por citomegalovirus. Estas observaciones realizadas en sangre son válidas para oras muestras biológicas como líquido amniótico o biopsia de tejidos. En gestantes que en la 21-25 semanas de edad gestacional tienen una carga viral elevada en líquido amniótico, el riesgo de transmisión al feto y el desarrollo de una infección sintomática es elevado. Otros estudios utilizando PCR en tiempo real han mostrado que la carga viral elevada en sangre y orina al nacer es habitual en recién nacidos infectados sintomáticos comparada con la de recién nacidos asintomáticos. Mas importante es que la carga viral en estos recién nacidos se relaciona con la futura pérdida auditiva sensorioneural.
La posibilidad de cuantificar el virus en sangre se ha convertido en un parámetro fundamental para decidir tratamiento y monitorizar la respuesta al tratamiento. En el contexto de medicina preventiva muchos centros adoptan la carga viral como parámetro para iniciar terapia. El umbral puede variar entre 1500-300.000 copias/ml, aunque en opinión de algunos autores la presencia de mas 10.000 copias/ml se asocia con peor respuesta al tratamiento, siendo en estos casos elevado el riesgo de experimentar un segundo episodio de replicación viral, por lo que puede ser necesario otro ciclo de tratamiento.
En Claire Atkinson y Vincent C. Emery (1); pueden consultarse algunos de los elementos comentados en este artículo.
Los citomegalovirus son virus muy especializados en infectar especies animales específicas, de esta forma los citomagalovirus humanos no pueden infectar a otros mamíferos como el ratón o el cerdo; de hecho, los citomegalovirus del cerdo o el ratón tienen una dotación genética sustancialmente diferente de la del citomegalovirus humano. Es un conocimiento de reciente adquisición que la activación de la inmunidad innata es un precisa para obtener respuesta de la inmunidad adquirida de calidad. Este proceso incluye la producción de interferón, la activación de células presentadoras de antígenos y células NK. La unión del citmegalovirus a la células y el paso a su interior inicia la producción de factor 3 regulador de interferón que activa la producción de interferón y citokinas inflamatorias. La respuesta de la inmunidad innata celular se pone en marcha tras la activación de los receptores Toll Like tipo 2 (TLR2), este receptor reconoce las proteínas gB y gH del virus. Las células NK son células del sistema de inmunidad innata que se caracterizan por la ausencia de los marcadores CD3 T y CD19 B; estas células juegan un papel importante en el control precoz de las infecciones virales. En las células infectadas por citomegalovirus parece tener lugar una disminución de la expresión de las moléculas de histocompatibilidad de clase I, lo que en última instancia originaría una reducción de los mecanismos de reconocimiento de las células NK. Se ha descrito que el citomegalovirus expresa un homólogo viral del antígeno de histocompatibilidad clase I, que se une a los receptores inhibitorios de las células NK, inhibiéndose por tanto la activación de estas células.
El papel de los anticuerpos específicos frente a citomegalovirus en el control de la reactivación y diseminación del virus esta poco claro. Tras producirse la primoinfección se liberan anticuerpos frente a las diferentes rpoteinas del virus, incluidas la proteínas de la cubierta pp65 y pp150 y las glicoproteinas de gB y gH, los anticuerpos frente a estas glicoproteínas se han relacionado con la capacidad de neutralizar el virus. El recuento de linfocitos T CD8 se ha relacionado con la capacidad de evitar una infección por citomegalovirus letal. Los linfocitos T CD8 parecen poseer receptores para la proteína de la cubierta del citomagalovirus pp65.
Citomegalovirus utiliza diversos mecanismos que interfieren con el procesamiento de los antígenos de histocompatibilidad de clase I, lo que dificulta el reconocimiento por los linfocitos T CD8. Ver Sarah E. y cols. (2).
El CMV es un herpesvirus cuyo genoma consiste en una doble tira de ADN, y que sólo crece en fibroblastos humanos. Existen dos o tres tipos de CMV, por lo que potencialmente puede padecerse más de una citomegalovirosis. La infección por CMV está ampliamente extendida, en especial ante condiciones higiénico-sanitarias deficientes. Una vez adquirida la infección, el virus es eliminado durante meses o incluso años a través de la orina y la saliva, lo que favorece su difusión; posteriormente se hace latente y podrá reactivarse en situaciones diversas.
Cada año aproximadamente el 1% de las mujeres susceptibles se seroconvierten durante el embarazo. Aunque la infección por vía genital puede ocurrir, lo habitual es el contagio a través de saliva, orina o fomites contaminados, incluidos juguetes. La citomegalia congénita corresponde a la infección prenatal por el citometalovirus (CMV), debida a la primoinfección de la mujer gestante y al paso transplacentario del virus hacia el embrión o el feto. Aproximadamente el 40% de las gestantes infectadas transmiten la infección al feto, de forma mas frecuente cuando ésta tiene lugar en el tercer trimestre de gestación. Sin embargo, cuanto más precozmente se presenta la infección, más desfavorable resulta el pronóstico para el recién nacido.
Es posible que la afectación exista en embarazos posteriores, aunque con menor gravedad, ya que la inmunidad humoral no protege completamente. Las reinfecciones pueden manifestarse durante el embarazo, tras enfermedades debilitantes o intervenciones quirúrgicas y al administrar inmunosupresores.
La citomegalia perinatal corresponde a la infección intranatal (contagio en el canal del parto donde la madre presenta recidivas locales de su enfermedad) o posnatal precoz (contagio por transfusiones sanguíneas, leche materna de banco contaminada o por vía respiratoria).
La infección por CMV es la más frecuente de las infecciones víricas en la gestante y en el recién nacido. Aproximadamente el 40% de las embarazadas son susceptibles a la infección por CMV, y entre el 1-4% de las mismas padecerán la primoinfección a lo largo de la gestación; un 40% transmitirá el CMV al feto. Por lo tanto, la infección congénita afectará al 1% de los recién nacidos, si bien sólo presentarán formas sintomáticas de la enfermedad el 10%.
La infección adquirida en el momento del parto tendrá lugar en el 2-6% de recién nacidos y habitualmente será asintomática. El riesgo postransfusional es del 1-8%, y la infección por leche materna se presenta en el 30-70% de los casos si la lactancia dura más de un mes y el recién nacido no dispone de anticuerpos anti-CMV.
Citomegalia congénita.
La forma sintomática grave aparece en uno de cada 10.000-20.000 recién nacidos (generalmente pretérminos o de bajo peso), que presentan la triada de ictericia, púrpura y esplenomegalia. Otros signos son distrés respiratorio, exantema maculopapuloso, vómitos, diarrea, convulsiones y ascitis. El cuadro clínico puede ser rápidamente mortal hasta en un 30%. Si el recién nacido sobrevive, la hepatoesplenomegalia persistirá unas semanas y, en un 90% de los casos, se detectarán secuelas neurológicas moderadas o graves con microcefalia o hidrocefalia, coriorretinitis o atrofia óptica, hipocalcificación del esmalte dentario, sordera neurosensorial, convulsiones y retraso psicomotor.
Se han descrito malformaciones congénitas asociadas como: comunicaciones intracardiacas, atresia de esófago o vías biliares, luxación congénita de cadera, cataratas, tetralogía de Fallot, megacolon… .
La forma sintomática, presente en el 90% de los casos, también puede condicionar secuelas neurológicas en el 5-15%, en especial hipoacusia y retraso mental discreto.
Citomegalia perinatal.
La forma adquirida en el canal del parto cursa con un distrés respiratorio (bronquitis, neumonitis intersticial) apareciendo a partir de las 3 semanas de vida. No suele haber afectación del SNC. La infección por leche contaminada suele ser asintomática. La forma adquirida por transfusión se presenta sobre todo en prematuros hijos de madre seronegativa que han recibido más de 50 ml de sangre.
La clínica aparece entre 3 y 5 semanas después, con hepatosplenomegalia, palidez grisácea, neumonitis, afectación hepática, trombocitopenia, anemia hemolítica y síndrome mononucleósico con adenopatías, exantema y linfocitosis absoluta y atípica. La afección dura 2-3 semanas, si bien fallece alrededor del 25% de los lactantes afectados.
Lo habitual en la citomegalia perinatal es que no quede ninguna secuela neurológica.
Exámenes Complementarios.
En sangre es frecuente una anemia hemolítica intensa con eritroblastosis, trombopenia y neutrofilia. El LCR presenta a menudo xantocromía, algunos eritrocitos, aumento de proteínas y posibles células gigantes. Es habitual la presencia de hiperbilirrubinemia y aumento de enzimas hepáticas. En ocasiones puede aparecer un síndrome de coagulación intravascular diseminada.
En la radiografía de cráneo suelen presentarse calcificaciones intracraneales, especialmente periventriculares, que pueden apreciarse mejor en la tomografía axial computadorizada (TAC) craneal. El examen de fondo de ojo puede mostrar una coriorretinitis. También pueden objetivarse déficit inmunitarios y lesiones óseas semejantes a las de la rubéola congénita.
El virus se aísla mediante cultivo en sangre, LCR y orina, en la cual persiste hasta 2 años, y es el método ideal de screening. El aislamiento del virus en la dos primeras semanas es demostrativo de infección congénita, ya que no existe en la infección perinatal.
La comprobación de una IgM específica elevada en el feto o recién nacido es diagnóstica de infección, y en la embarazada de primoinfección. En cuanto a los anticuerpos IgG fluorescentes indirectos o detectados mediante prueba de fijación del complemento o inhibición de la hemaglutinación, un título estable en los 6 primeros meses es típico de infección congénita, mientras que la infección perinatal mostrará un descenso durante los 2-3 primeros meses, seguido de un aumento posterior.
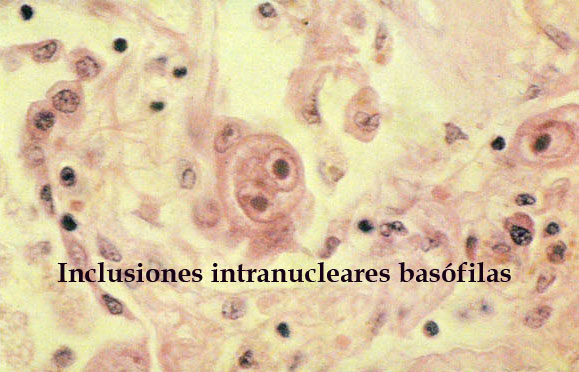
La visualización de células gigantes con núcleo excéntrico e inclusiones intranucleares e intracitoplasmáticas (células en «ojo de búho» o en «ojo de lechuza») en orina, LCR, saliva, jugo gástrico o biopsia hepática ayudan a establecer el diagnóstico; pueden estar ausentes en el 25% de los casos.
El análisis del ADN vírico en orina tiene gran utilidad para los estudios epidemiológicos pero aún no se encuentra al alcance del clínico.
Diagnóstico Diferencial.
Se efectuará con el resto de infecciones prenatales (sobre todo rubéola congénita, toxoplasmosis congénita, sífilis congénita y herpes simple generalizado), sepsis del recién nacido, isoinmunización Rh grave y neumonía afebril del lactante pequeño.
Siguiendo a Cruz Hernández; en el recién nacido se deberá hacer siempre un diagnóstico diferencial entre las entidades que cursen con ictericia, hepatoesplenomegalia, púrpura y afectación neurológica, así podemos distinguir:
a) Rubéola Congénita: Hay clínica semejante a la del CMV: ictericia, hepatoesplenomegalia, exantema petequial o purpúrico, microcefalia y afectación neurológica. Sin embargo no hay calcificaciones intracerebrales y el antecedente de infección en el primer trimestre del embarazo y las pruebas virológicas sugerirán el diagnóstico.
b) Toxoplasmosis: Hay hepatoesplenomegalia, coriorretinitis y caldificaciones intracraneales. NO suele cursar con lesiones purpúricas ni petequiales. El estudio virológico y la presencia de células de inclusión en orina apoyarán el diagnóstico de CMV.
c) Herpes simple generalizado: Cursa con ictericia, hepatoesplenomegalia y afectación neurológica. No suele haber calcificaciones intracraneales. Suele iniciarse con la erupción herpética generalizada con afectación de mucosa bucal y conjuntival.
d) Sífilis congénita: También hay hepatoesplenomegalia, ictericia, alteraciones neurológicas . No hay calcificaciones intracraneales y se acompaña a Rx de osteitis luética.
e) Sepsis del recién nacido y eritroblastosis fetal: También cursa con ictericia, hepatoesplenomegalia y púrpura. Loa cultivos o antecedentes e compatibilidad y test de Coombs aclararán el diagnóstico.
Respuesta inmunológica a la infección.
Los citomegalovirus son virus muy especializados en infectar especies animales específicas, de esta forma los citomagalovirus humanos no pueden infectar a otros mamíferos como el ratón o el cerdo; de hecho, los citomegalovirus del cerdo o el ratón tienen una dotación genética sustancialmente diferente de la del citomegalovirus humano. Es un conocimiento de reciente adquisición que la activación de la inmunidad innata es un precisa para obtener respuesta de la inmunidad adquirida de calidad. Este proceso incluye la producción de interferón, la activación de células presentadoras de antígenos y células NK. La unión del citmegalovirus a la células y el paso a su interior inicia la producción de factor 3 regulador de interferón que activa la producción de interferón y citokinas inflamatorias. La respuesta de la inmunidad innata celular se pone en marcha tras la activación de los receptores Toll Like tipo 2 (TLR2), este receptor reconoce las proteínas gB y gH del virus. Las células NK son células del sistema de inmunidad innata que se caracterizan por la ausencia de los marcadores CD3 T y CD19 B; estas células juegan un papel importante en el control precoz de las infecciones virales. En las células infectadas por citomegalovirus parece tener lugar una disminución de la expresión de las moléculas de histocompatibilidad de clase I, lo que en última instancia originaría una reducción de los mecanismos de reconocimiento de las células NK. Se ha descrito que el citomegalovirus expresa un homólogo viral del antígeno de histocompatibilidad clase I, que se une a los receptores inhibitorios de las células NK, inhibiéndose por tanto la activación de estas células.
El papel de los anticuerpos específicos frente a citomegalovirus en el control de la reactivación y diseminación del virus esta poco claro. Tras producirse la primoinfección se liberan anticuerpos frente a las diferentes rpoteinas del virus, incluidas la proteínas de la cubierta pp65 y pp150 y las glicoproteinas de gB y gH, los anticuerpos frente a estas glicoproteínas se han relacionado con la capacidad de neutralizar el virus. El recuento de linfocitos T CD8 se ha relacionado con la capacidad de evitar una infección por citomegalovirus letal. Los linfocitos T CD8 parecen poseer receptores para la proteína de la cubierta del citomagalovirus pp65.
Tratamiento.
Se efectuará aislamiento estricto del recién nacido. No está justificada la supresión de la lactancia materna. Actualmente puede resultar útil el Ganciclovir a dosis de 5 mg/kg/dia durante 2 semanas, si bien puede provocar exantemas, leucopenia, aplasia y, a largo plazo, quizás esterilidad. Otros fármacos utilizados son el inteferón y el factor de transferencia. También se dispone de gammaglobulina hiperinmune, que se puede administrar a dosis de 400 mg/Kg los días 0, 4 y 8 con adición de 200 mg/Kg los días 12 y 16.
Profilaxis.
Debido a la relativa baja incidencia y poca gravedad de la enfermedad adquirida intraparto, no está justificada la práctica de cesárea sistemática ante la sospecha de citomegalia genital, a diferencia de lo que ocurre con el herpes. No obstante, como entre un 50-80% de los donantes de sangre son seropositivos y la infección se transmite por los leucocitos infectados, el método que se recomienda actualmente es la utilización de filtros de leucocitos en todas las transfusiones de sangre o plaquetas. La utilidad de la inmunoglobulina hiperinmune, que ha demostrado su utilidad para evitar la transmisión vertical y horizontal de hepatitis B o varicela, permanece controvertida cuando su indicación es la infección por citomagalovirus de la gestante. P. Duff (3); analizan las evidencias existentes sobre la utilidad de la inmunoglobulina hiperinmune en gestantes con primoinfección por citomegalovirus. Las dosis utilizadas oscilan entre 100-200 U/Kg y la utilidad en los estudios existentes hasta el presente (observacionales) parece clara.
Dr. José Uberos Fernández
Hospital Clínico San Cecilio, Granada
REFERENCIAS
(1) Atkinson C, Emery VC. Cytomegalovirus quantification: Where to next in optimising patient management? Journal of Clinical Virology 2011;51(4):223-8.
(2) Jackson SE, Mason GM, Wills MR. Human cytomegalovirus immunity and immune evasion. Virus Research 2011;157(2):151-60.
(3) Duff P. Immunotherapy for congenital cytomegalovirus infection. N Engl J Med 2005 Sep 29;353(13):1402-4.